¿Qué elementos tienen la mayor electronegatividad?
Hemera Technologies/PhotoObjects.net/Getty Images
Al investigar la naturaleza de los enlaces químicos, el químico Linus Pauling desarrolló la idea de la electronegatividad en 1932. Asignó a los elementos un número desde el 4, para el flúor, hasta 0,7, para el cesio, basado en la habilidad para atraer a los electrones de los átomos vecinos. Elementos con un número alto atraen con mayor fuerza a los electrones. Puedes predecir muy de cerca la electronegatividad de un elemento por su posición en la tabla periódica.
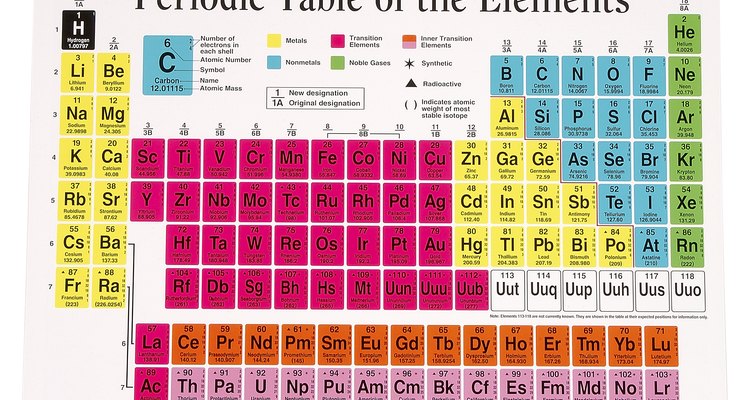
Tabla periódica
Conforme avanzas de la izquierda a la derecha en la tabla periódica, y de abajo hacia arriba, los números de la electronegatividad de los elementos se incrementan. Es más alto para los elementos halógenos, como el flúor y el cloro, y más bajo para los metales alcalinos, como el sodio y el litio. Debido a la complejidad de las cargas eléctricas en los diferentes elementos, esta es una guía general, no una regla absoluta. Aunque el oxígeno no es un elemento halógeno, su electronegatividad está cerca a la del flúor.
Moléculas polares
Los elementos que tienen la mayor diferencia en los números de electronegatividad tienden a formar moléculas polares. Estas moléculas tienen un exceso de carga negativa de un lado y carga positiva del otro. El agua es un buen ejemplo de una molécula polar, ya que la fuerte electronegatividad del oxígeno jala los electrones del hidrógeno hacia él. Esto expone al único protón del hidrógeno y su carga positiva. El carbono y el oxígeno, al ser vecinos en la tabla periódica, tienen una electronegatividad similar. El dióxido de carbono tiene una mucho menor polaridad que la del agua.
Proyección
Conforme vas de arriba hacia abajo en la tabla periódica, los elementos tienen una electronegatividad menor. Entre más electrones en estos elementos rodeen el núcleo con carga positiva, se proyectan sus efectos de atracción. Átomos más simples en la parte superior de la tabla tienen menos electrones para proyectar el núcleo, así que los protones atraen con más fuerza, incrementando la electronegatividad.
Sistemas diferentes
Pauling no fue el único científico en trabajar con la idea de la electronegatividad. Otros, como A.L. Allred y E.G Rochow, refinaron la idea en términos de la atracción desde el núcleo del átomo y los electrones externos. Al contrario de los números atómicos obvios, como el número de protones, el número de la electronegatividad puede calcularse en diferentes formas. El sistema de L.C. Allen tiene al neón como el elemento con la más alta electronegatividad, teniendo al flúor como segundo muy de cerca al primero.
Más artículos
¿Qué es un grupo de átomos que se unen y actúan como una sola unidad?→

¿Cómo diferenciar el azúcar alfa del beta?→

Cómo calcular la polaridad entre dos elementos mediante electronegatividad→

Efectos de los elementos de aleación en el acero→

¿Cómo difiere un compuesto iónico de un compuesto molecular?→

¿Cómo dibujar la estructura atómica de los átomos?→
Referencias
Sobre el autor
Chicago native John Papiewski has a physics degree and has been writing since 1991. He has contributed to "Foresight Update," a nanotechnology newsletter from the Foresight Institute. He also contributed to the book, "Nanotechnology: Molecular Speculations on Global Abundance."
Créditos fotográficos
Hemera Technologies/PhotoObjects.net/Getty Images
